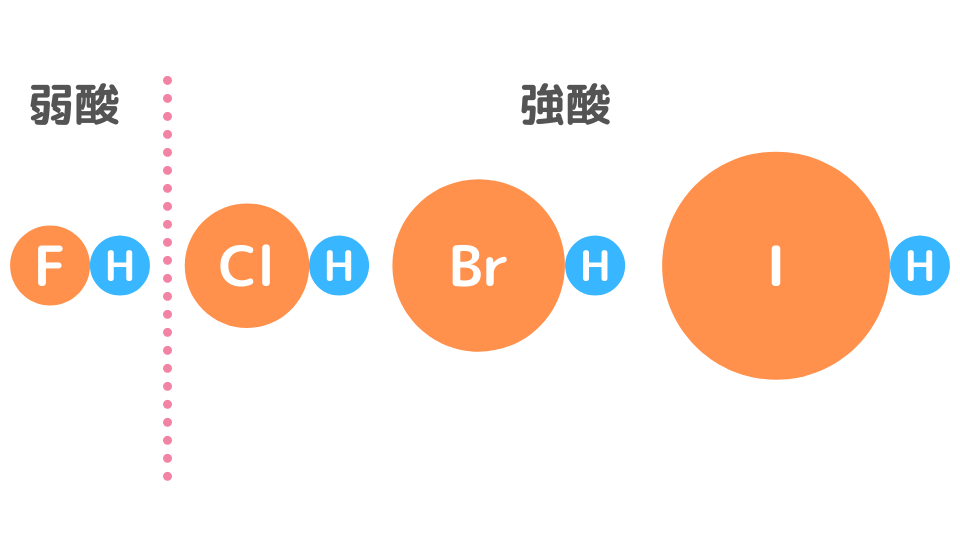
HCl、HBr、HIは強酸ですが、ハロゲン化水素の中でHFだけは弱酸です。なぜでしょう。
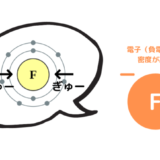
Fはハロゲンの中で最も原子半径が小さいです。そのため、正電荷を持つ原子核が電子を強く引きつけ、電子密度が高い状態(負電荷が集中している状態)になります。
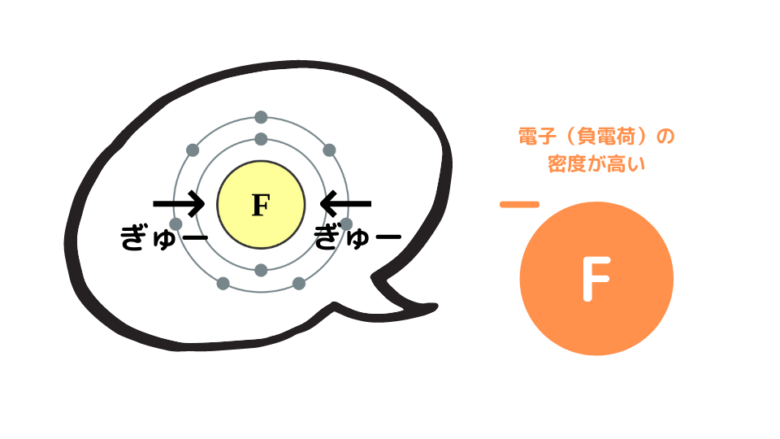
その結果、H+を強く引き寄せ、さらにHF同士で水素結合を形成し、H+が電離しづらくなります。
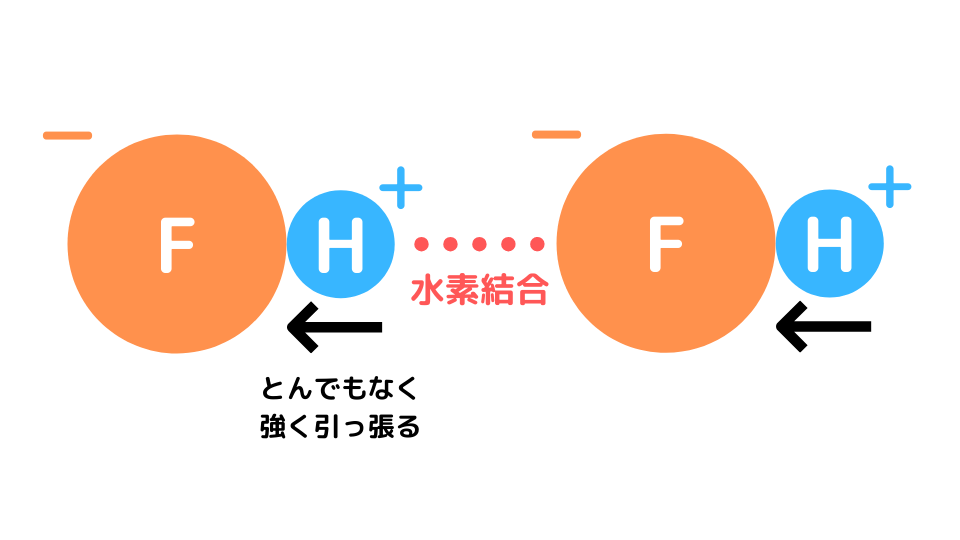
HClの場合には、原子半径が大きいため電子密度はそこまで大きくならず、H+を強く引き寄せません。その結果、H+は電離し強酸となります。H+が電離しているため、水素結合を形成しません。
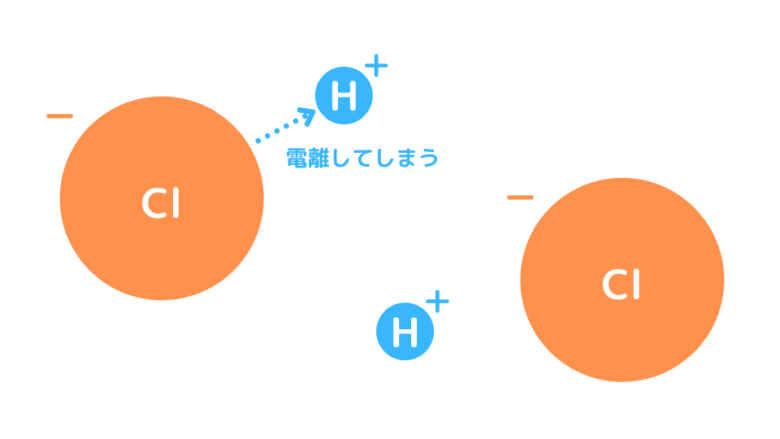

フッ化水素は水素結合を形成するから、融点も沸点も高くなるよ。