H2OもHFもNH3もどれも水素結合を形成する分子です。水素結合の強さ順は電気陰性度の大きさによって決定するので、HF、H2O、NH3となっています。
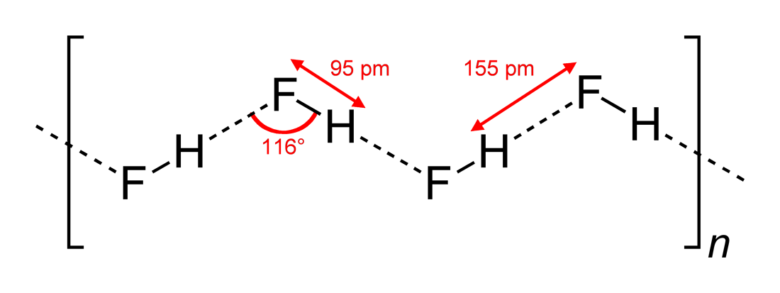
H2OがHFよりも沸点が高い理由は、水素結合の数です。HFは1つの分子につき2つしか水素結合を形成しませんが、H2Oは4つの水素結合を形成します。そのため、H2Oの方が水素結合を切るのにエネルギーが必要となり、沸点がHFよりも大きくなります。

ちなみにNH3は水素結合も弱いし、水素結合の数も2つだから3者の中では沸点は1番低いんだね!

H2OもHFもNH3もどれも水素結合を形成する分子です。水素結合の強さ順は電気陰性度の大きさによって決定するので、HF、H2O、NH3となっています。
H2OがHFよりも沸点が高い理由は、水素結合の数です。HFは1つの分子につき2つしか水素結合を形成しませんが、H2Oは4つの水素結合を形成します。そのため、H2Oの方が水素結合を切るのにエネルギーが必要となり、沸点がHFよりも大きくなります。

ちなみにNH3は水素結合も弱いし、水素結合の数も2つだから3者の中では沸点は1番低いんだね!