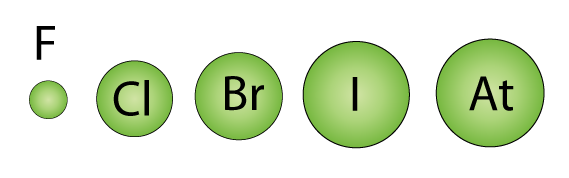
ハロゲン元素の中ではフッ素は原子半径が一番小さいです。そのため、原子核の正電荷が最外殻電子殻に強く働き、他から電子を引き寄せる力(酸化力)が強くなります。
例えば、KBrの水溶液(K+とBr–を含む水溶液)にF2を吹きいれるとBr2が遊離します。これはFの方がBrよりも電子を奪う力が強いため、Br–から電子を奪ってしまうことによって起きます。
F2 + 2Br– → 2F– + Br2

酸化力(電子を奪う力)がより強い方が電子を奪って陰イオン化するんだね。
ハロゲン元素の中ではフッ素は原子半径が一番小さいです。そのため、原子核の正電荷が最外殻電子殻に強く働き、他から電子を引き寄せる力(酸化力)が強くなります。

例えば、KBrの水溶液(K+とBr–を含む水溶液)にF2を吹きいれるとBr2が遊離します。これはFの方がBrよりも電子を奪う力が強いため、Br–から電子を奪ってしまうことによって起きます。
F2 + 2Br– → 2F– + Br2

酸化力(電子を奪う力)がより強い方が電子を奪って陰イオン化するんだね。