Contents
タンパク質とは
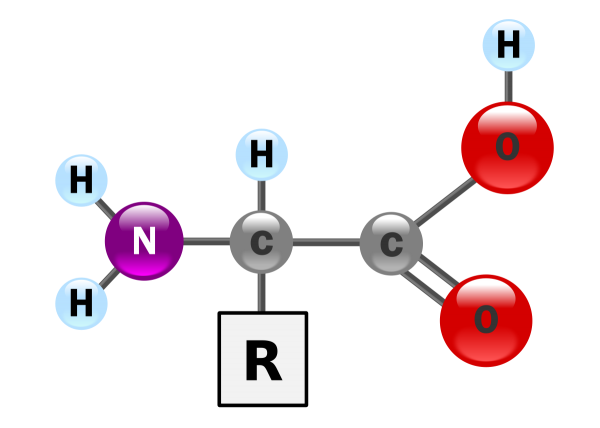
α-アミノ酸がペプチド結合で重合した物質をタンパク質(ポリペプチド)と呼ぶ。

タンパク質の構造
タンパク質には、一次構造、二次構造、三次構造、四次構造がある。
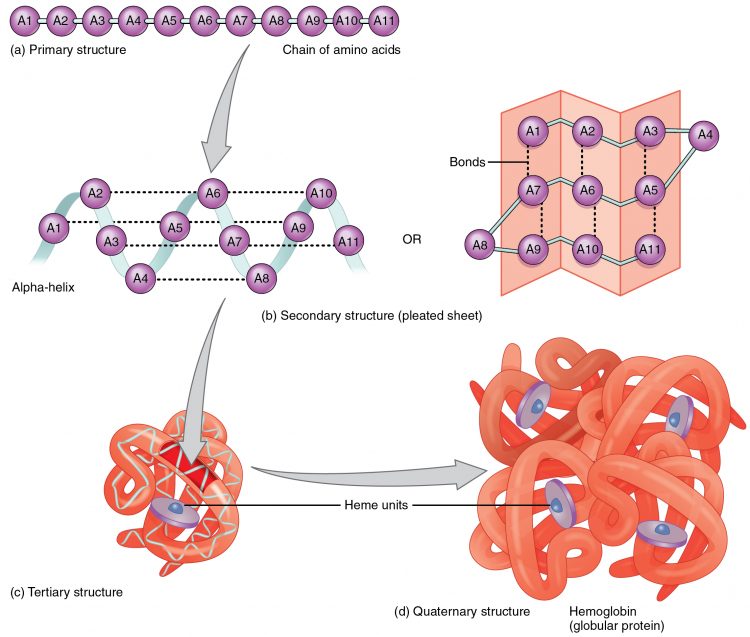
一次構造はα-アミノ酸の配列順序のことを指す。
二次構造は、アミノ酸の鎖(ポリペプチド)がらせん状、もしくはひだ状の構造を形成している様を指す。らせん状構造をα-ヘリックス、ひだ状構造をβ-シートと呼ぶ。
三次構造は、α-ヘリックスやβ-シート構造を持つポリペプチドが、折れ重なったりしている構造を指す。イオン結合、ジスルフィド結合などが関与している。
四次構造は、三次構造を持つポリペプチドが複数集合した様を指す。
タンパク質の結合
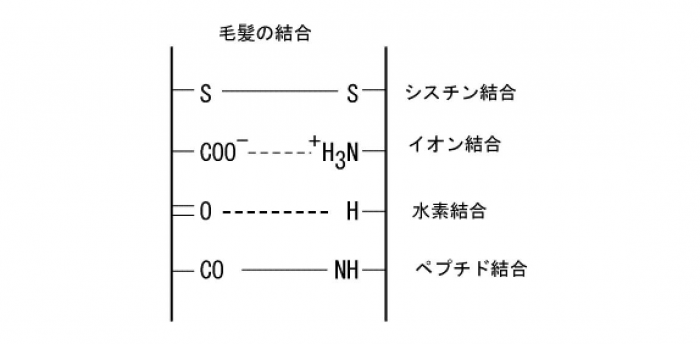
タンパク質同士はイオン結合やジスルフィド結合によって結合する。例えば、イオン結合では、グルタミン酸(負の電荷)とリシン(正の電荷)同士が結合したりする。
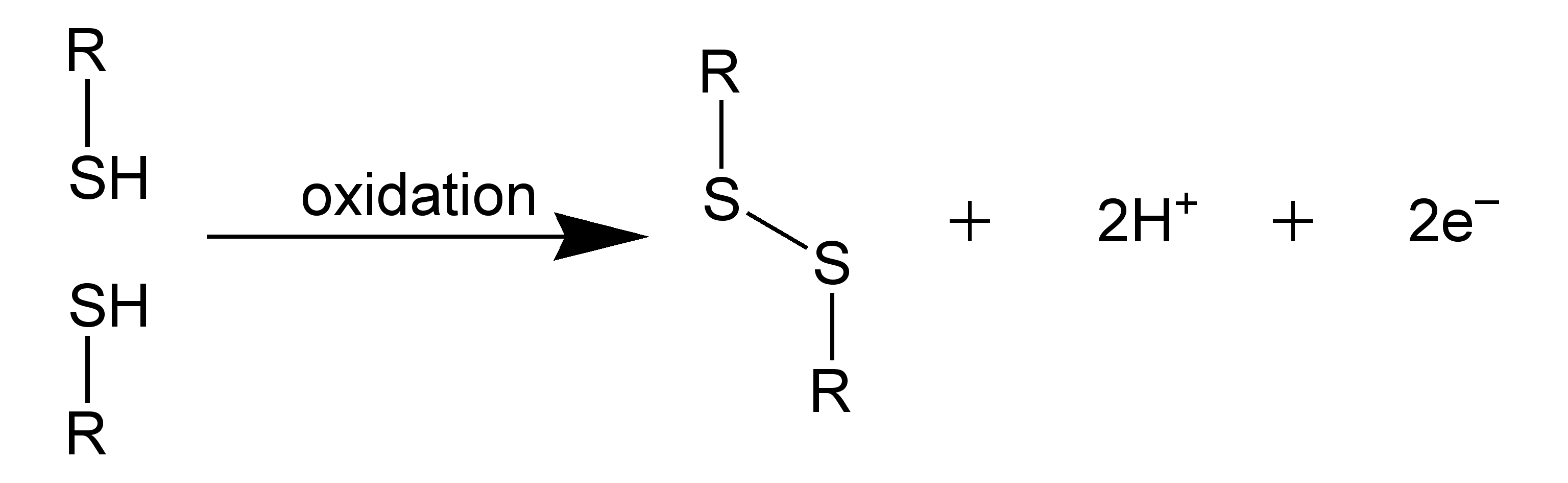
ジスルフィド結合は、2組のチオール(-SH)のカップリングで得られる共有結合である。-SH HS-の間からH2が取れ、-S-S-結合(ジスルフィド結合)を形成する。
タンパク質の分類
タンパク質は形状や構成成分によって分類されている。形状では繊維状か球状で区別され、構成成分では、単純か複合かで区別される。
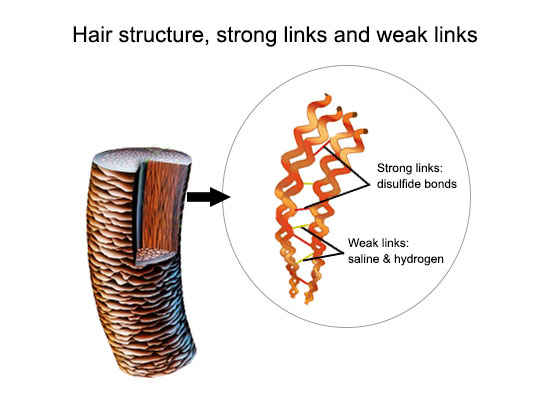
繊維状タンパク質
タンパク質が繊維状であり、ケラチン(毛、爪)、フィブロイン(絹)、コラーゲン(軟骨、けん)などの種類がある。
球状タンパク質
タンパク質が球状であり、アルブミン(水に可溶)、グロブリン(水に不溶)などがある。どちらも卵白の成分である。どちらも食塩水には可溶である。
タンパク質の性質
タンパク質の代表的な性質として、変性、塩析、加水分解の3つがある。
変性
タンパク質の二次構造以上の構造が破壊され、タンパク質の性質が変化することを変性と呼ぶ。一次構造は壊れにくい。
塩析
水溶性のタンパク質は分子量が大きいため親水性コロイドとして水溶している。そのため、多量の電解質を投入してやると、水和のために必要な水分子を電解質の方に取られてしまい、水に溶けることができなくなり、沈殿が生じる。この現象を塩析と呼ぶ。
加水分解
酸や塩基、酵素によって加水分解されやすい。

https://www.sciencedirect.com/
タンパク質の呈色反応
タンパク質を検出するために、呈色反応を用いることがある。呈色反応にはビウレット反応、キサントプロテイン反応、酢酸鉛(Ⅱ)との反応、ニンヒドリン反応がある。
ビウレット反応
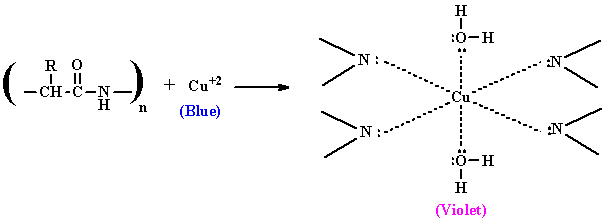
Cu2+とペプチド結合中のN原子が配位結合を形成して、錯イオン(赤紫色)を生じる反応である。そのため、2つ以上のペプチド結合があれば呈色が見られる。
https://infograph.venngage.com/
キサントプロテイン反応
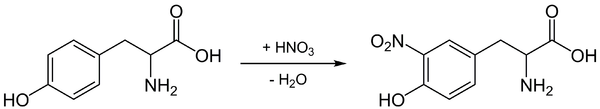
濃硝酸を加えて加熱すると黄色の呈色を示する。

タンパク質を構成するアミノ酸のうち、チロシン、フェニルアラニン、トリプトファンなど、ベンゼン環を持つもの(芳香族アミノ酸)がニトロ化されることで呈色反応が起きる。ゼラチンのようなベンゼン環を持つアミノ酸を含まないタンパク質は、この反応が起こらない。
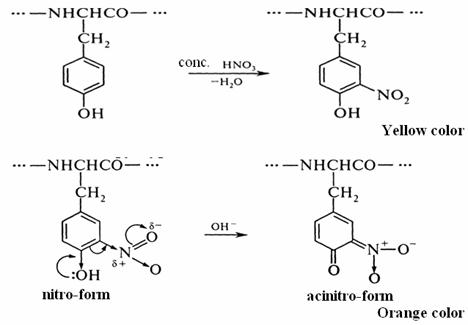
濃アンモニウム水またはアルカリをさらに加えるとニトロ化されたチロシンのフェノール性水酸基-OHがアルカリ性(pH9以上)でH+を遊離し、より波長の長い(428nm付近)の吸収率が大きくなる。そのため赤みを帯びて見える。
酢酸鉛(Ⅱ)との反応
固体の水酸化ナトリウムを加えて加熱し、酢酸鉛(Ⅱ)水溶液を加えると、硫化鉛(II)PbSの黒色沈殿が見られる。タンパク質に含まれる硫黄元素Sを検出している。
ニンヒドリン反応
ニンヒドリンを含む水溶液とタンパク質を共に加熱すると、ニンヒドリンがアミノ酸(アミノ基)と反応し、赤紫色に呈色する。
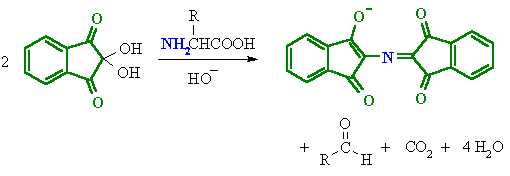
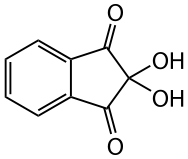
ニンヒドリンとは以下のような構造を持つ物質である。
その他のN原子の検出方法
また、タンパク質に含まれる窒素を検出するためには、NaOHを加えて熱しアンモニアを発生させ、HCl(気体)と反応させてNH4Clの白煙を確認する。
Делегація послів різних країн завітала до Державного податкового університету https://dpu.edu.ua/novyny/delehatsiia-posliv-riznykh-krain-zavitala-do-dpu