鉄の電子配置は、M殻(3番目の電子殻)のs軌道に2個、3d軌道に6個存在します。3d軌道は10個まで電子が入るため、まだ4つの空きがあります。
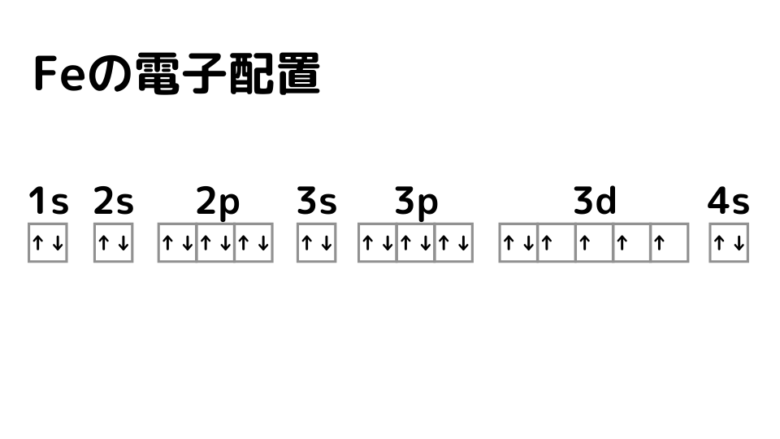
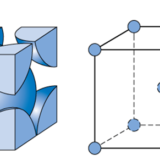
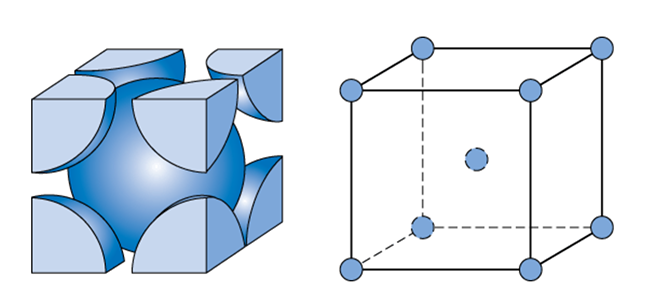
M殻の3d軌道に存在する6個の電子のうち、2個の電子はお互いが反対向きのスピンのペアになり磁性を打ち消し合いますが、残りの4個の電子はペアにならず孤立したスピンになります。鉄のd軌道には4個の未対合電子は、特定の方向に向かって結合する傾向があります。この方向性のある結合は、体心立方格子の形になることで最も安定になります。
面心立方格子や六方最密構造は、隙間が少なくて最密に詰まっている結晶構造ですが、鉄の場合は方向性のある結合が優先されるため、体心立方格子になります。

d軌道の電子の影響によって鉄の結晶構造が決定されていたんだね!