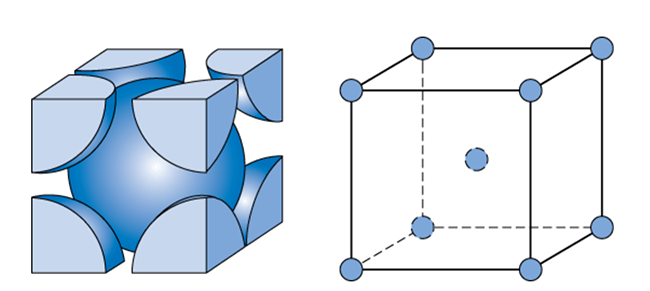
体心立方格子は面心立方格子や六方最密構造に比べて隙間がある結晶構造です。つまり、あまり原子同士が引きつける力が強くない原子が取りやすい結晶構造となっています。
金属結合は価電子の数が多いほど結合が強くなりますが、アルカリ金属は価電子が1つしかなく金属結合がとても弱いです。また、金属結合は自由電子を原子核が引きつけることによってお互いにくっつきあっていますが、アルカリ金属は原子半径が大きいために価電子を束縛する力が弱くなり、自由電子が非局在化しやすくなります。その結果さらに金属結合が弱くなります。
金属結合が弱まることにより、原子が熱の影響によって振動しやすくなります。このことから、アルカリ金属は隙間が多少ある体心立方格子をとっていると考えられています。

アルカリ金属の柔らかさからも金属結合の弱さがわかるよね!