実はアルコールもわずかに電離する「酸」の1つ
高校化学ではアルコールは電離しないと教えられます。しかし、実際にはごくわずかに電離します。
C2H5OH ⇔ C2H5O– + H+
しかし、アルコールの電離度は水のそれよりも小さいため、水の電離で生じたH+によって、アルコールの電離はほぼ抑えられています。そのため、溶液は中性になります。
フェノールはなぜ酸性?
フェノールはベンゼン環にヒドロキシ基が結合した物質です。同じヒドロキシ基を持つ物質なのに、フェノールはごく弱い酸性を示します。なぜでしょうか。
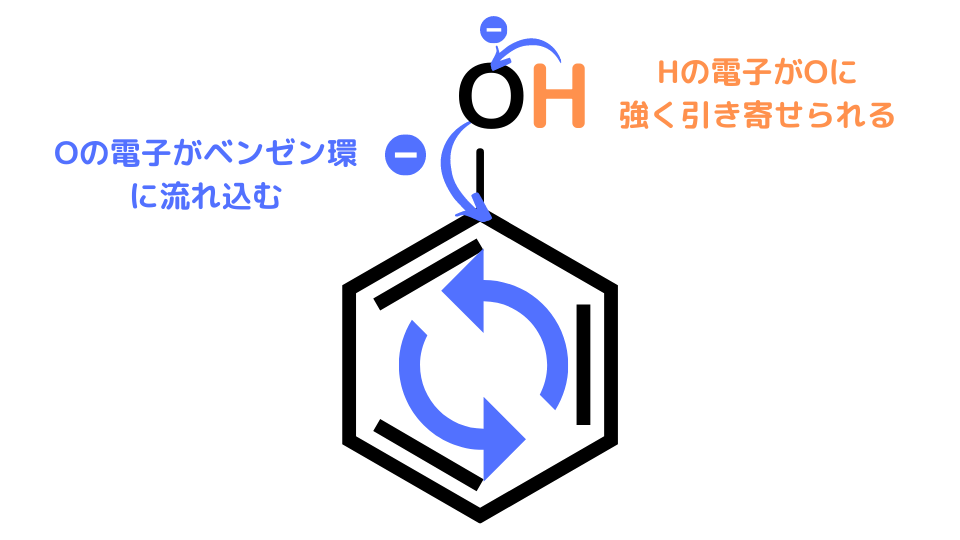
フェノールはOの電子がベンゼン環へ流れ込んで非局在化(グルグルまわって安定化)しています。その電子不足を解消するためにOはHから電子を奪い、HはH+として放出されやすくなります。
しかし、超弱酸であるヒドロキシ基が少し安定したぐらいなので、酸性は非常に弱く、青色リトマス紙を赤色に変えることすらできません。
ヒドロキシ基は実は電離しますが、とんでもなく電離度が低いです。そのためアルコールは中性を示します。
しかし、フェノールはベンゼン環があることによって電離している状態が幾分か安定化するため、非常に弱い酸性を示します。

質問です
アルコール100%の溶液のPHはどうなるのでしょか。
水のPHは水のイオン積から7というのはわかりますが、そもそも水溶液でない場合どうなるのでしょうか
フェノール100%だと電離することができなく、水素イオン濃度は0になります!(電離という現象は水があることによって起こります)。また、pHはあくまで「水溶液」中の水素イオン濃度を指すため、100%フェノールではpHという表し方はできません。