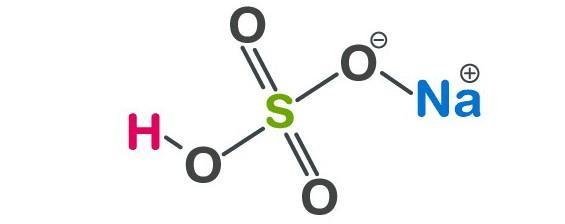
塩の加水分解では「強酸と強塩基の中和反応でできた塩=中性」というイメージが強いです。しかし。水酸化ナトリウムと硫酸の中和反応によってできた硫酸水素ナトリウムの水溶液は酸性になります。これは塩の加水分解ではなく、単純にNaHSO4の電離によるためです。
NaHSO4 → Na+ + H+ + SO42-
塩の加水分解を考慮したとしても、NaHSO4から電離した分のH+が多くなり、液性は酸性だということがわかります。
NaHSO4 + H2O → Na+ + H+ + SO42- + H+ + OH–
一方、炭酸水素ナトリウムは塩の加水分解によって水溶液は塩基性になります。これは弱酸の炭酸が電離しにくいためですね。
NaHCO3 + H2O → Na+ + H2CO3 + OH–

NaHCO3のHは炭酸が弱酸だから電離しにくいんだね!一方、NaHSO4のHは硫酸が強酸だから電離してしまうよ!