希薄溶液
希薄溶液とは十分に濃度の薄い溶液のことを指す。溶質の種類によらず、蒸気圧降下、沸点上昇、凝固点降下などの現象が見られる。
蒸気圧降下
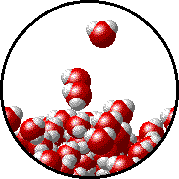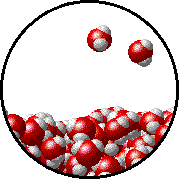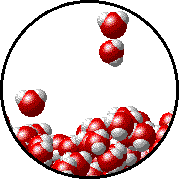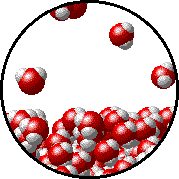
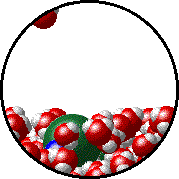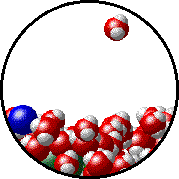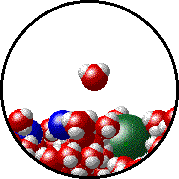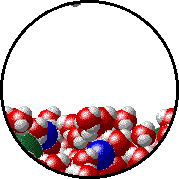
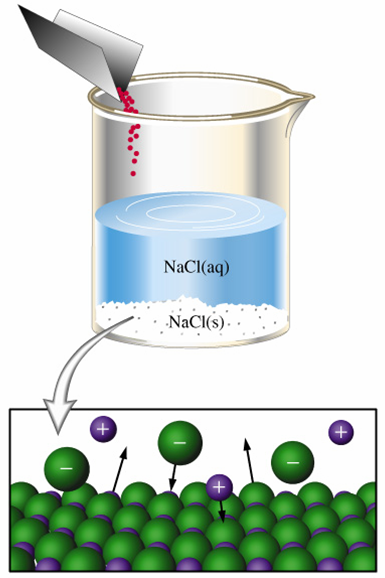
NaClなどの不揮発性の電解質を溶かした溶液の蒸気圧は、何も溶かしていない溶液の蒸気圧よりも低くなることが知られている。この現象を蒸気圧低下と呼び、溶液の濃度に比例する。
溶質が邪魔で蒸発しにくいhttp://catalog.flatworldknowledge.com/
蒸気圧
液体分子が蒸発しようとする時に空気を押し上げる力。水は0.02気圧ほどある。油などは蒸気圧が非常に低いので蒸発しにくい。
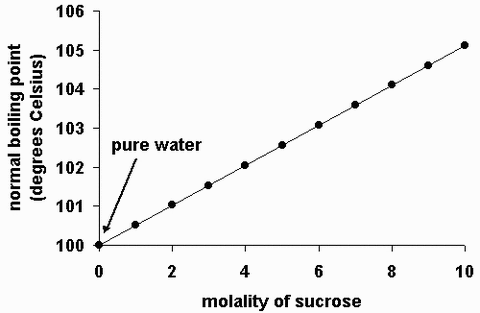
沸点上昇
何かが溶けている液体(溶液)は、何も溶けていない液体に比べ沸点が上昇する。このことを沸点上昇と呼ぶ。上昇率は溶液の質量モル濃度に比例する。
凝固点降下
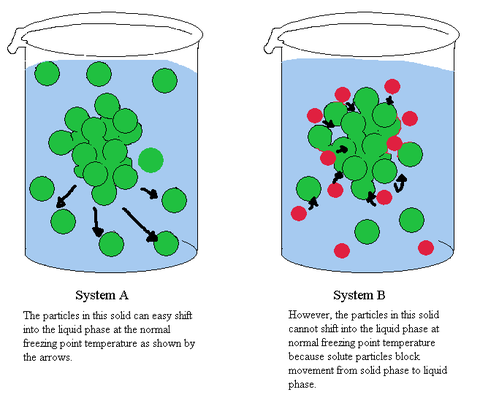
何かが溶けている液体(溶液)は、何も溶けていない液体に比べ固体になる温度が降下する。この現象を凝固点降下と呼ぶ。降下率は溶液の質量モル濃度に比例する。
溶液(右)はきれいな配列を作ることができず凝固点が降下するhttp://www.scienceiscool.org/
溶質の分子量の求め方
沸点上昇度(どれくらい沸点が上昇したか)または凝固点降下度(どれくらい凝固点が降下したか)が溶液の質量モル濃度に比例する性質を利用し、 溶質の分子量を求めることができる。
沸点上昇度(⊿t) はモル沸点上昇k(K・kg/mol)に質量モル濃度m(mol/kg)を掛けることによって求めることができる。
![]()
質量モル濃度mは、溶質の質量w(g)/溶質の分子量M×1000/溶媒の質量W(g)で求めることができる。これを上記の式に代入し、M=の形に直すと次のようになる。
M = 1000kw / W・Δt
モル沸点上昇
物質1モルを溶質として、溶媒1000グラムに溶かした溶液の沸点の上昇度。溶質の種類によらず、溶媒に固有の定数となる。