飽和溶液
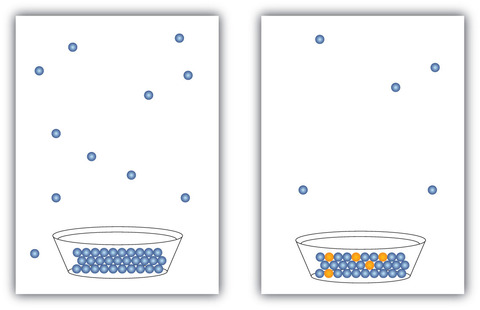
これ以上溶けることができなくなった溶液をと呼ぶ。飽和溶液の中に結晶が生じている場合、見かけ上は結晶の大きさは変化しないが、粒子レベルでは溶け出したり析出したりと繰り返している。このような実際は粒子が動いているのにも関わらず、その粒子の出入りの量が等しい状態を溶解平衡と呼ぶ。
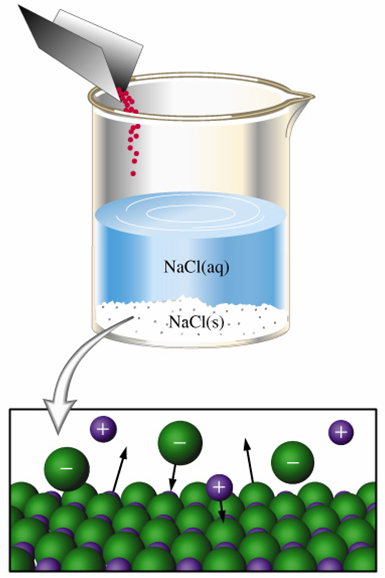
飽和溶液では溶解平衡が起こるhttp://dluetgens.com/
溶解度
固体の溶解度
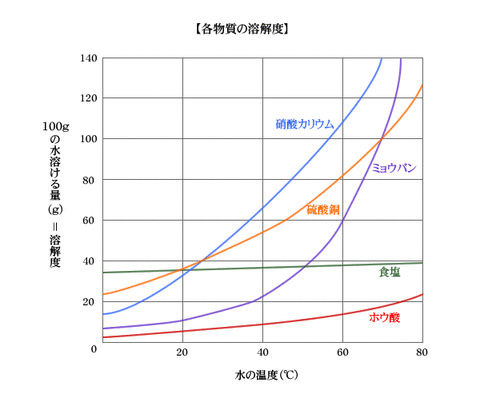
溶媒100gに限界まで溶かすことができる溶質の質量gを、その固体の溶解度と呼ぶ。温度が高くなると液粒子が活発に動き、溶質を多く溶かすことができるようになるため溶解度は大きくなる。結晶水を含む物質は、無水物の質量gに直して計算する。
固体の溶解度の変化は右肩上がりhttp://chemistry1.juniorhighschool-science.net/
気体の溶解度
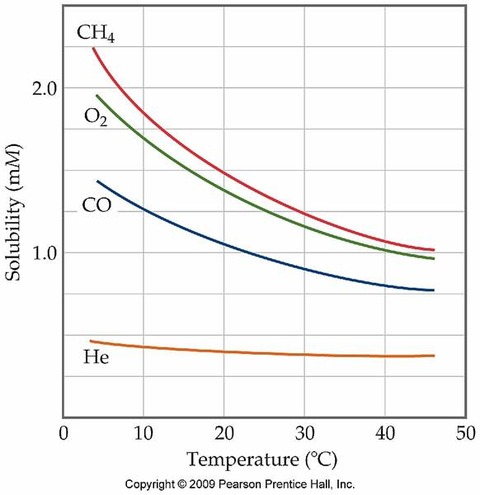
1013hPaの状態で気体が溶媒1mlに溶解することができるその気体の体積mlを気体の溶解度と呼ぶ。温度が高くなるほど分子の動き活発となって気体分子が飛び出るので溶解度は小さくなる。
気体の溶解度の変化は右肩下がりhttp://staff.norman.k12.ok.us/
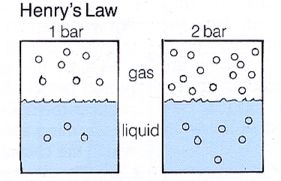
ヘンリーの法則
気体の圧力が大きくなればなるほど、たくさんの気体分子が溶媒に溶けることができるという法則。混合気体では、各気体の分圧によって溶けやすさが決定する。
実験で確かめよう
準備
試験官、ビーカー、温度計、水10ml、ミョウバン7g
実験方法
- 試験官に水10mlを入れ、ミョウバンを1g入れて、温度計でかき混ぜる。
- 溶けない場合は、湯煎にして温める。
- 完全に溶けきったら温度を記録し、火を止め、 ミョウバンを1gずつ加えていく。
- 溶けない場合には、火を付けて湯煎の温度を上げる。 完全に溶けきった温度を記録する。
- ミョウバンが7g完全に溶けるまで実験を続ける。
- 実験が終わったら、冷水に浸してついでに結晶が析出する様子を見る。
結論
温度に比例して溶解度が上昇していく。グラフ化するとなお良い。