弱酸(弱塩基)の遊離
弱酸由来の塩に強酸を加えると、弱酸が遊離する反応が起こる。
CH3COONa + HCl → NaCl + CH3COOH
弱酸は電離度が低いため、イオンの状態よりも分子の状態を好む。一方、強酸はイオンの状態を好む。そのため、強酸のH+は弱酸由来のイオン(CH3COO-)に奪われる。弱塩基に強塩基を加えても同様の反応が起こる。
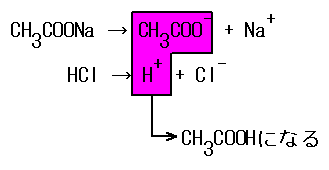
http://www.geocities.jp/
揮発性の酸の遊離
揮発性とは蒸発のしやすさという意味である。揮発性の酸由来の塩に、不揮発性の酸を加えると、不揮発性の酸由来の塩を形成し、より安定しようとする。その結果、揮発性の酸は遊離する。
NaCl(揮発性酸の塩) + H2SO4(不揮発性酸) → NaHSO4 +HCl
NaCl(揮発性酸の塩) + H2SO4(不揮発性酸) → NaHSO4 +HCl
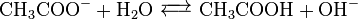

Plaeisng to find someone who can think like that