Contents
極性分子である
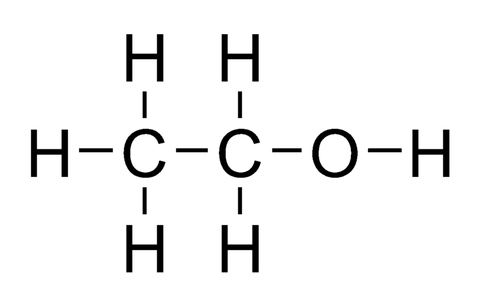
炭素数3までのアルコールは水によく溶ける。それ以上の炭素数は溶けづらい。OHがあるが、共有結合でがっつり結びついているため電離しない。そのため、中性となる。

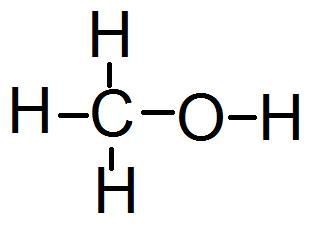
Hの電子がOに引きつけられて+となり、Oは-に帯電する。
第1級アルコールは酸化するとアルデヒドになる
第一級アルコールにOが結合し、その後H2Oが離れるとアルデヒド(CHO)が生成される。トータルでHを2つ失うこととなるため、酸化である。
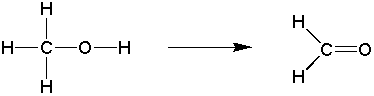
メタノールが酸化されるとホルムアルデヒドとなる。
第2級アルコールは酸化するとケトンになる
第二級アルコールにOが結合し、その後H2Oが離れるとケトン(CO)が生成される。トータルでHを2つ失うこととなるため酸化である。
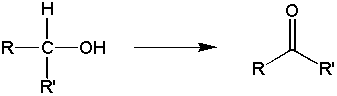
COをケトン基と呼ぶ。
ナトリウムと反応しナトリウムアルコキシドを生成する
OHのHが電離し、ONa(イオン結合)を形成する。水素が発生する。ナトリウムメトキシド、ナトリウムエトキシド、ナトリウムプロポキシドなどがある。いずれも、ノールの前の音をお行にして命名する。
アルコール分子内で脱水するとアルケンを生成する
2重結合が形成される。分子内での脱水を脱離と呼ぶ。
アルコール分子間で脱水するとエーテルを生成する
エーテル結合(-O-)が形成される。分子間での脱水を縮合と呼ぶ。
カルボン酸と脱水反応してエステルを生成する
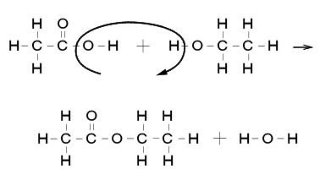
カルボン酸(COOH)がOH、アルコール(OH)がHを出してH2Oを失い、エステル結合COOを形成する。

That inigsht’s perfect for what I need. Thanks!