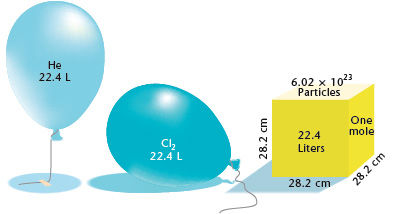
気体1molの体積
標準状態(0℃、1013hpa)において、どのような気体であっても1molは22.4Lであると決まっている。1molの時の体積をモル体積と呼ぶ。
アボガドロの法則
どのような気体であっても 同温・同圧では同数の分子を含むという考えをアボガドロの法則と呼ぶ。
気体の分子量
気体の分子量は密度から求めることができる。
例:密度2.0g/L(標準状態)の気体の分子量
2.0g/L × 22.4L=44.8g
1mol(22.4L=1mol)の時に44.8gなので、44.8g/mol。
1molの時の質量は、その分子量に等しいので、分子量=44.8。
混合気体の平均分子量
混合気体の平均分子量は次のように求めることができる。
例:空気はN2:O2=4:1で構成されている。
N2の分子量=28
O2の分子量=32
28 × 4/5 + 32 × 1/5 = 28.8g/mol
よって、空気の平均分子量=28.8