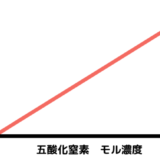
希薄溶液では粒子の大きさはそこまで大きな影響を与えないから
水溶液では、純粋な水に比べて沸点が上昇したり、凝固点が降下したりします。その程度は溶質の種類には関係なく、溶質の質量モル濃度に比例します。なぜ溶質の種類に関係ないのでしょう。
そもそも、溶液では溶質の分だけ溶媒分子の割合が減少するため、溶液の表面から蒸発する溶媒分子が少なくなり蒸気圧が降下します。この蒸気圧降下によって沸点が上昇します。
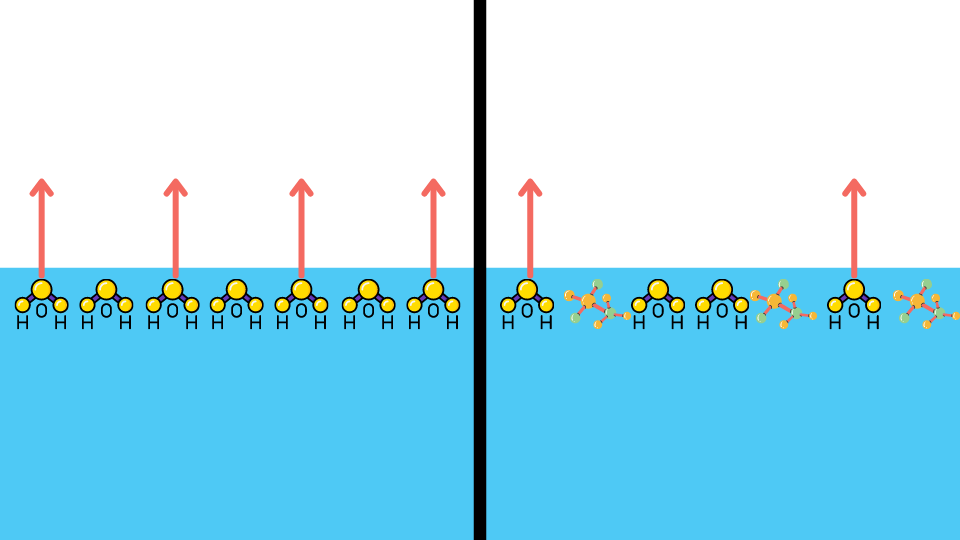
溶質の粒子は非常に微小であり、分子やイオンの大きさの違いはありますが、希薄溶液ではそもそも粒子の数が少ないため、溶質の粒子の大きさ(溶質の種類)は殆ど影響を与えません(厳密にいえば極わずかには影響を与えています)。
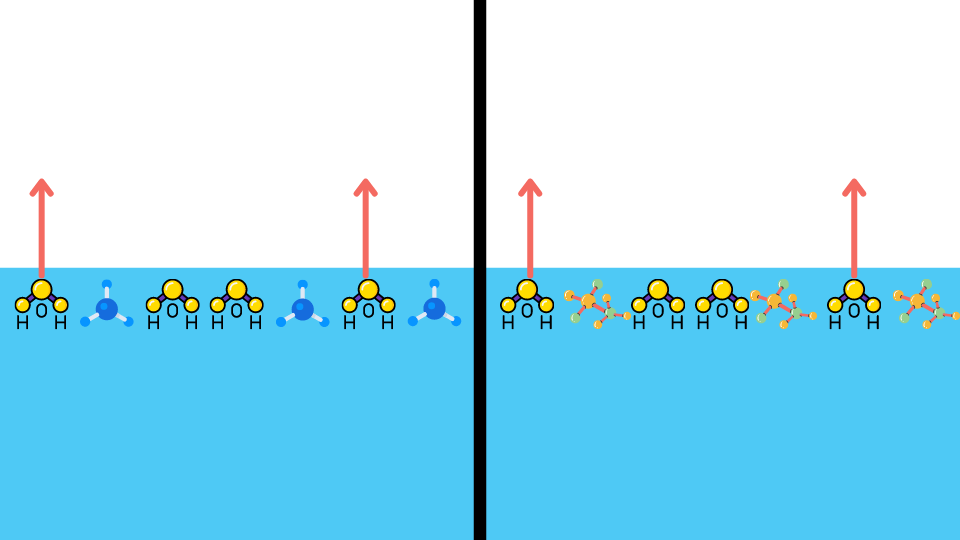

これが希薄溶液ではない濃い溶液ならば話は別です。あくまで希薄溶液の話。ちなみに希薄溶液の目安は0.1mol/Lほどです。