ナトリウムのハロゲン化物の融点はそれぞれNaF 993℃、NaCl 801℃、NaBr 747℃となっています。一方二族元素の酸化物は、MgO 2826℃、CaO 2572℃、BaO 1918℃となっており、ナトリウムのハロゲン化物よりも遥かに高いです。
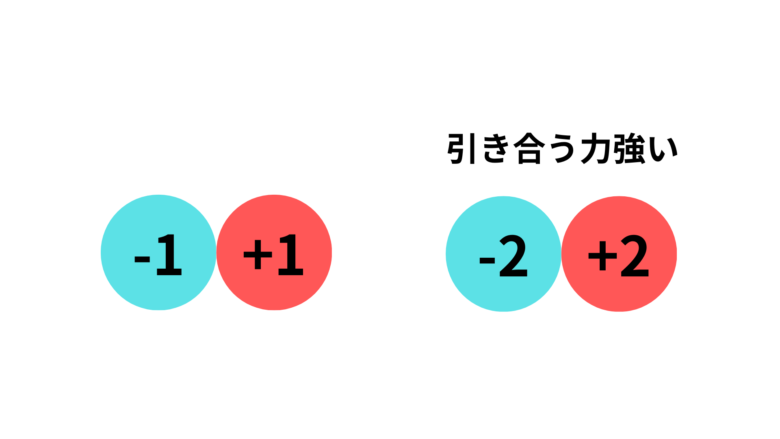
ナトリウムのハロゲン化物は一価の陽イオンと一価の陰イオンが結合した物質です。一方、二族元素の酸化物は二価の陽イオンと二価の陰イオンが結合しており、それぞれに強いクーロン力(電気的に引き付け合う力)が働き、より融点が高くなります。

元素1つあたりのイオン結合で引き合う力が強くなるんだね!

