NaClの溶解熱の吸熱量はそこまで大きくないから
多くの固体の溶解度は温度が上がれば大きく上昇しますが、NaClは僅かにしか上昇しません。これは、NaClの溶解熱と関係があります。
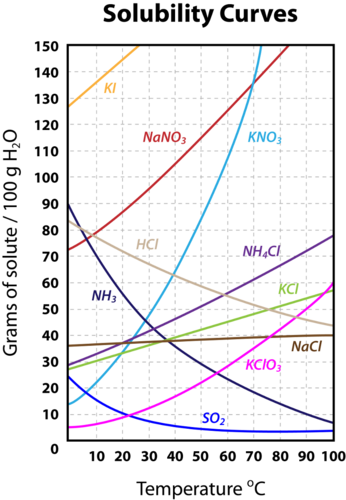
例えば、KNO3とNaClの溶解熱を比べると次のような違いがあります。
KNO3(固)+ aq ⇔ K+aq + NO3–aq -34.9kJ
NaCl(固)+ aq ⇔ Na+aq + Cl–aq -3.9kJ
どちらも吸熱反応なので、熱すると反応が右側に傾きます(つまり溶けやすくなります)。しかし、NaClの吸熱量はそこまで大きくないため、熱しても反応が右側にあまり傾かないのです。