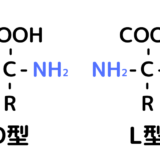
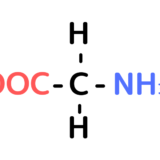
カルボキシ基とアミノ基の電離度の差があるから
アミノ酸はカルボキシ基(酸)とアミノ基(塩基)のどちらも持つ物質です。そのため、分子内で中和反応が起こり、双性イオンとして存在します。この反応は中和反応ですので、双方の電離度に関係なく起こります。
双性イオンはさらに水と反応します(塩の加水分解のようなもの)。グリシンを例に考えてみましょう。
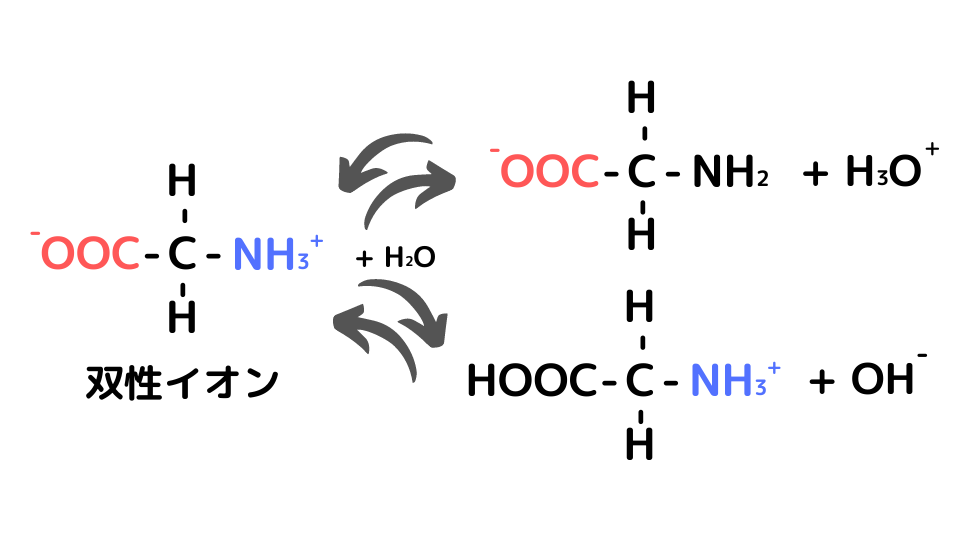
中性(pH=7)の環境では、実際には上段の物質(グリシン陰イオン)の方が若干多く、グリシン陽イオンとグリシン陰イオンは同量ではありません。これは、カルボキシ基とアミノ基の電離度の差があるためです。そのため、上段の反応を逆向きにするように少しH+(H3O+)を増やしてやります。
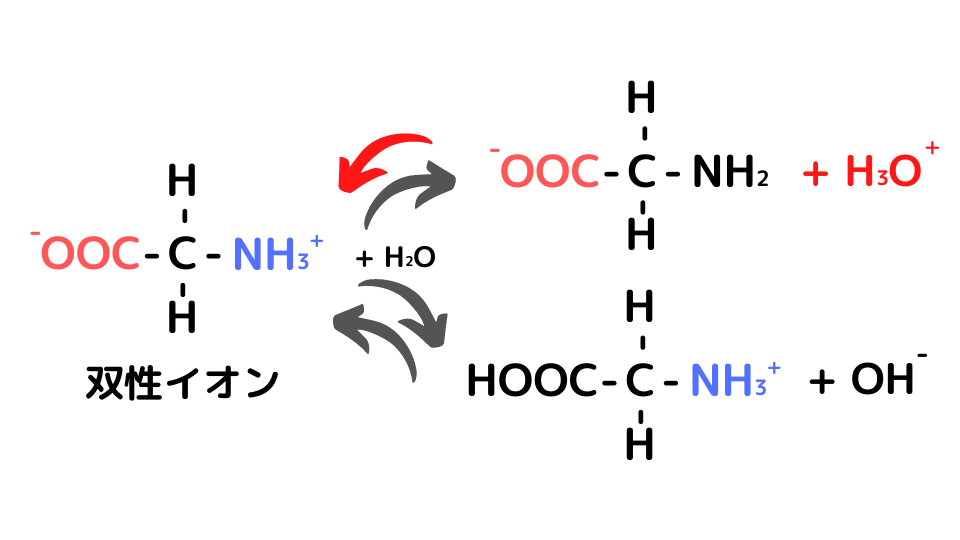
すると、溶液は酸性になりますがグリシン陰イオンの量が減ります。グリシン陰イオンとグリシン陽イオンの量が調度同じになる点を探してやると、pHは6になります。

分子内の中和反応ではカルボキシ基とアミノ基は同じ分だけ反応するけど、その後に起こる水との反応で量に差が出てくるんだね。