状態変化
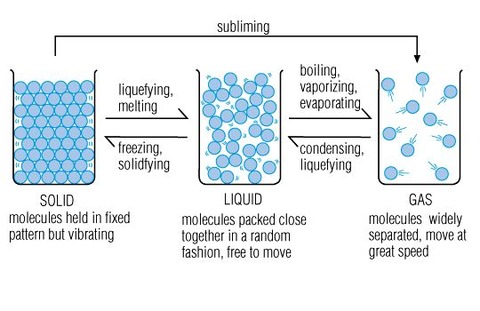
三態の変化にはそれぞれ名前が付けられている。
- 気体→(凝縮)→液体→(凝固)→固体
- 気体←(蒸発)←液体←(融解)←固体
- 気体←(昇華)←固体
- 気体→(昇華)→固体
状態変化と熱量
状態変化には熱の移動が伴う。
融解熱
ある物質が1mol融解するのに必要な熱量。水の場合は6kJ/molである。
蒸発熱
ある物質が1mol蒸発するのに必要な熱量。水の場合は41kJ/molである。
熱量
物質ごとに1℃(Kでも良い)上昇するために必要なエネルギー(熱量)は測定されており、それを比熱と呼ぶ。ある物質の質量mグラムに熱量を加えて、t℃(Kでも良い)上昇した際m熱量は次の式で求めることができる。
Q = mct
Q(熱量J) = m(質量g)×c(比熱J/(g・k))×t(変化した温度k)
熱い量はまことで覚えると良い。