亜鉛 Zn
性質
銀白色の金属である。酸にも塩基にも溶ける両性金属(両性元素)である(Al Zn Sn Pbは両性金属、「ああすんなり」と覚えよう)。
Zn + 2HCl → ZnCl2 + H2
https://www.youtube.com/watch?v=sJhoYABoprA
Zn + 2NaOH → Na2[Zn(OH)4] (テトラヒドロキシド亜鉛(Ⅱ)酸ナトリウム )+ H2
亜鉛はトタン、乾電池の材料に使われる。銅と亜鉛の合金は黄銅(真鍮)と呼ぶ。

酸化亜鉛 ZnO
性質
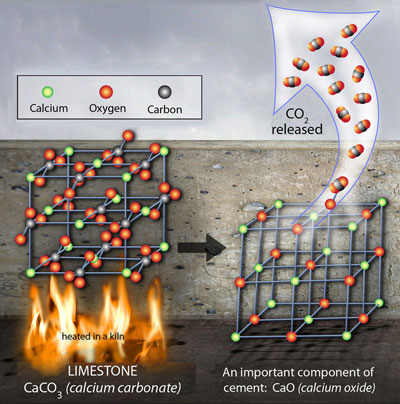
白色粉末であり、白色顔料、軟こうとして用いられる。亜鉛を酸化することで得られる。
2Zn + O2 → 2ZnO

https://what-is-nanotechnology.com/
両性酸化物(酸・塩基とも塩を生成する酸化物)である。
ZnO + 2HCl → ZnCl2 + H2O
ZnO + 2NaOH + H2O → Na[Zn(OH)4]
水酸化亜鉛 Zn(OH)2
性質
白色固体であり、両性水酸化物である。
Zn(OH)2 + 2HCl → ZnCl2 + 2H2O
Zn(OH)2 + 2NaOH → Na2[Zn(OH)4]
また、アンモニア水に溶けて錯イオンを形成する。
Zn(OH)2 + 4NH3 → [Zn(NH3)4]2+ + 2OH–