水酸化銀を形成するけどすぐに酸化銀に変化してしまう
銅イオンCu2+は水酸化物イオンOH–と反応して水酸化銅Cu(OH)2の沈殿を生じますが、銀イオンAg+は水酸化物イオンOH–と反応すると酸化銀Ag2Oの沈殿を生じます。これはなぜしょう。
Cu2+ + 2OH– → Cu(OH)2
2Ag+ + 2OH– → Ag2O + H2O
実は、銀イオンも水酸化物イオンと反応して水酸化銀AgOHを生じます。しかし、水酸化銀はすぐに酸化銀Ag2Oに変化してしまうのです。

反応機構を見ていきましょう。
Agは電気陰性度(電子を引っ張る力)が高く、Ag-O間ではそこまで極性が大きくなりません。その結果、O-H間の極性が大きくなり、他のAgOHと水素結合を形成します。
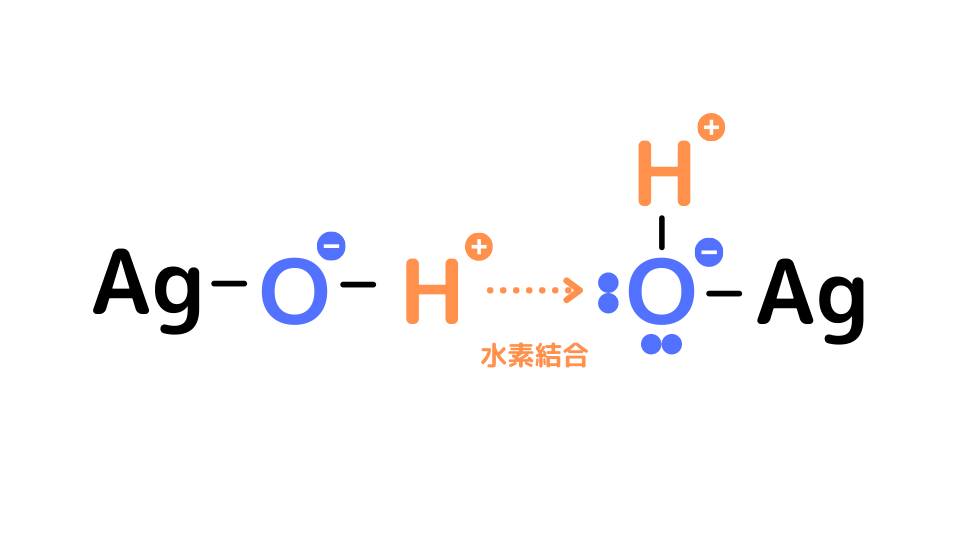
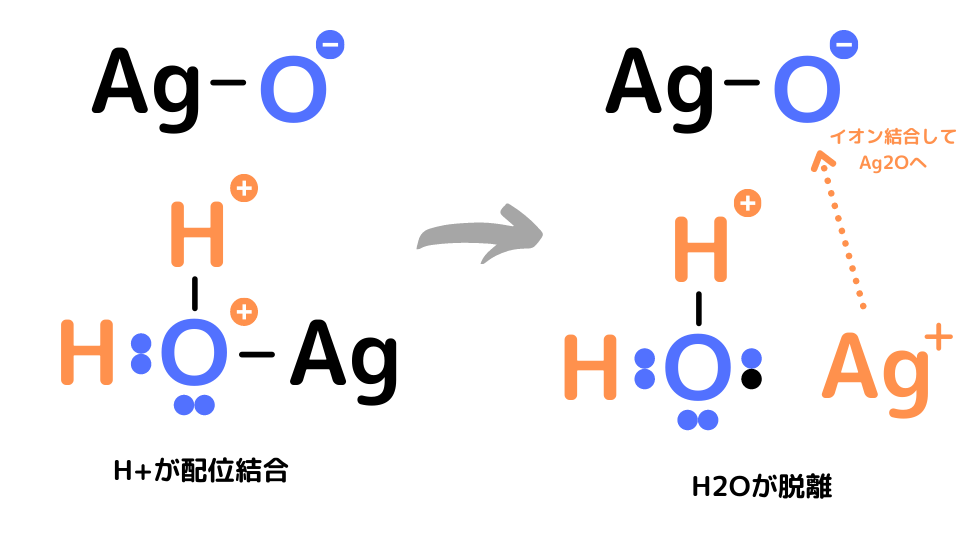
そしてH+の移動が起こり、水H2Oが脱離します。残されたAg+はAgO–と結合してAg2Oになります。

ちなみに銀は電気陰性度が高いから分極しなくて化合物は殆ど沈殿するよ。電気陰性度の高さが銀の色んな性質に関わっているんだね。

でも銀と銅の電気陰性度って同じぐらいなんじゃないんですか?
銀よりも電気陰性度が大きい金属は沢山あることが引っ掛かります。教えて頂きたいのですが、、
銀よりも電気陰性度が低いHgなども、やはり水酸化物が非常に不安定で、HgOにすぐ変わってしまいます。
返信遅くなりすみません。
銅もやはり水酸化物は不安定なので、酸化銅に変化します。しかし、Agよりは安定しているため、熱する必要があります。僅かな差ですが、化学的性質には結構差がでます(銅と銀が別の金属的性質を持つように)。