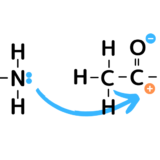
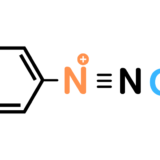
アニリンを希塩酸に溶かして氷冷したものに亜硝酸ナトリウム水溶液を加えると塩化ベンゼンジアゾニウムが生成されます。

反応機構を見ていきましょう。
まず、亜硝酸ナトリウム水溶液と希塩酸が反応し、弱酸の遊離反応によって亜硝酸(弱酸)が遊離します。
NaNO2 + HCl → NaCl + HNO2

亜硝酸はとても不安定な弱酸。そのため、亜硝酸ナトリウムと塩酸を反応させてその場で生成しなければならいんだ。
亜硝酸イオンは弱酸のため、強酸HCl存在下ではブレインステッドの塩基として働き、H+を受け取って(Oに配位結合させ)H2Oを脱離し、NO+が作られます。
HNO2 + H+ → NO+ + H2O
生成されたNO+がアニリン分子のNの非共有電子対を攻撃します。
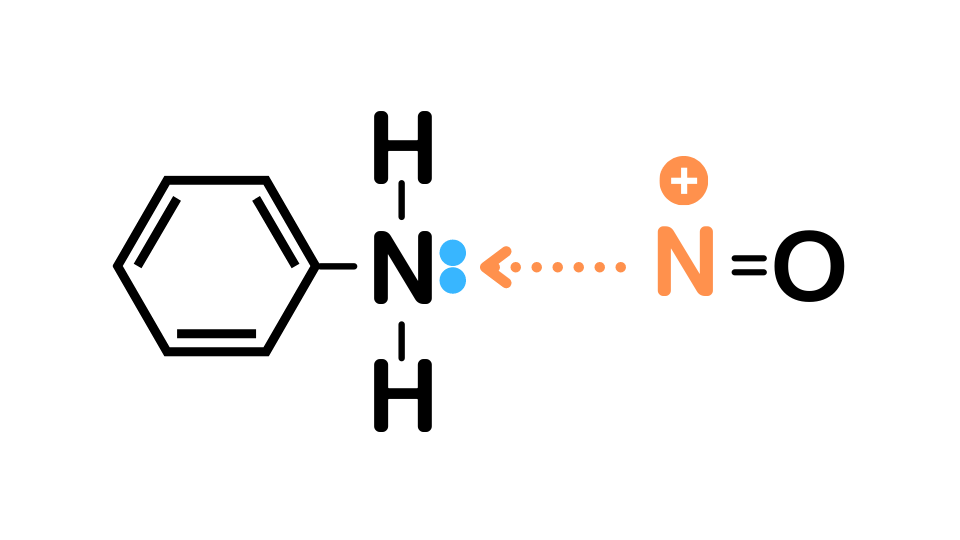
その結果、配位結合が形成されます。電子を供給した左側のNが正の電荷を持ちます。
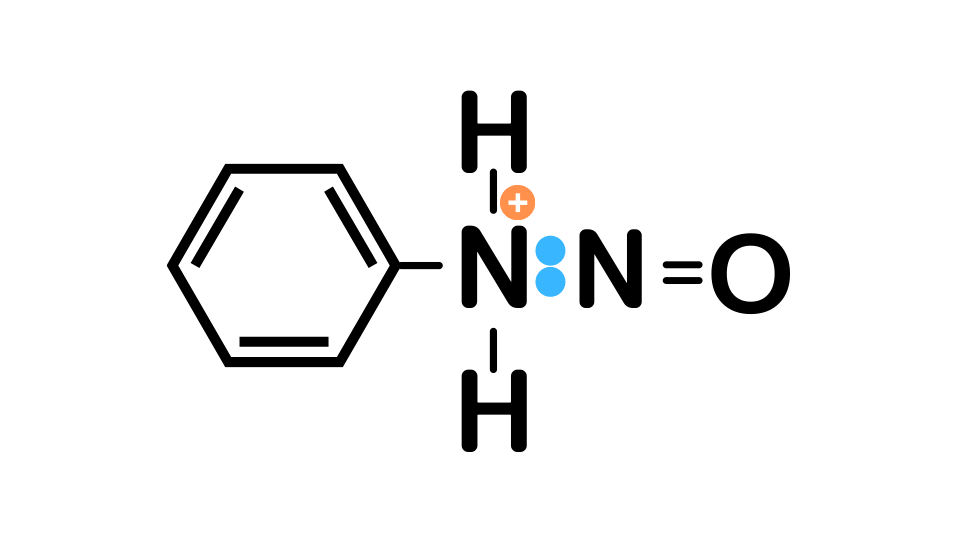
さらにH2Oが脱離し塩化ベンゼンジアゾニウムが生成されます。
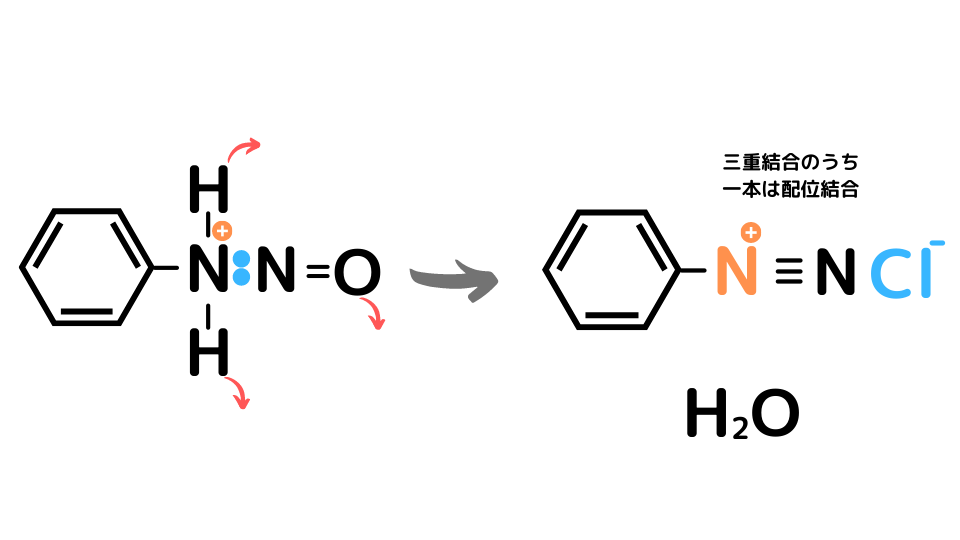

真ん中のNがプラスになっているのは、NOと配位結合したなごりなんだね。
これはただの書き方の問題です。実際は、N+にベンゼン環から電子が供給されてベンゼン環全体がプラスの電荷を帯びているような状態になっています。そのため、「端のN」とイオン結合をしているというよりも、ベンゼンジアゾニウムイオン全体とイオン結合をしているという理解が正しいです。
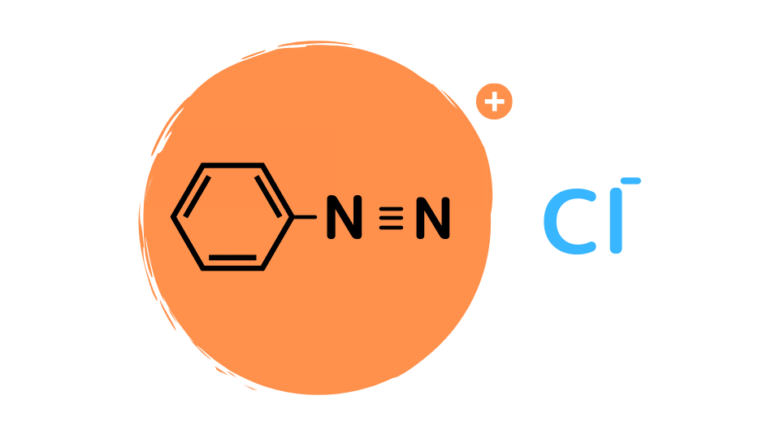
塩化ベンゼンジアゾニウムは非常に不安定な物質で、常温では加水分解が起こって窒素が脱離してフェノールに変化してしまいます。そのため、氷冷下で反応をさせないといけないのです。
加水分解反応は、まず塩化ベンゼンジアゾニウムからN2から脱離し、フェニル陽イオンが生成されます。

フェニル陽イオンに水分子が攻撃し、最終的にH+が脱離してフェノールが生成されます。
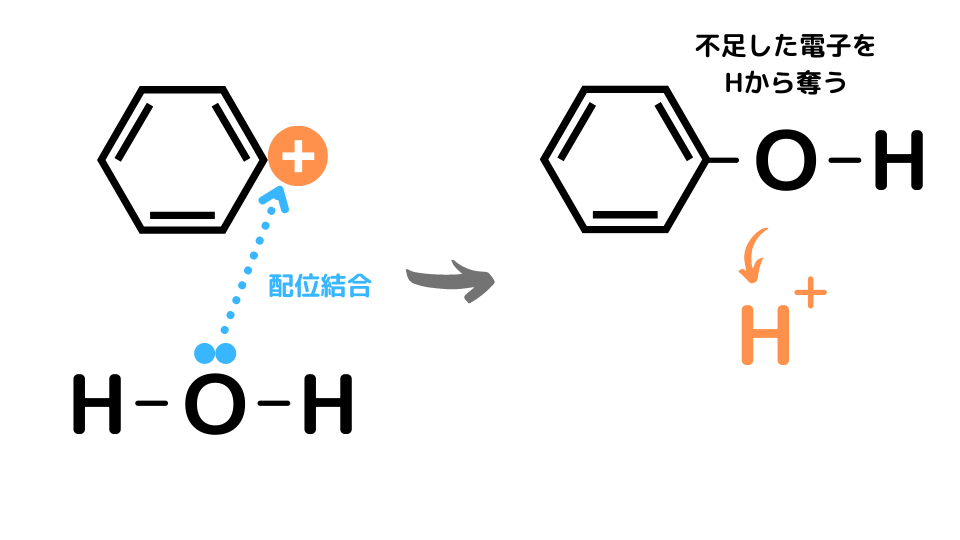

ベンゼンジアゾニウムイオンはとても不安定な物質であることを覚えておこう。