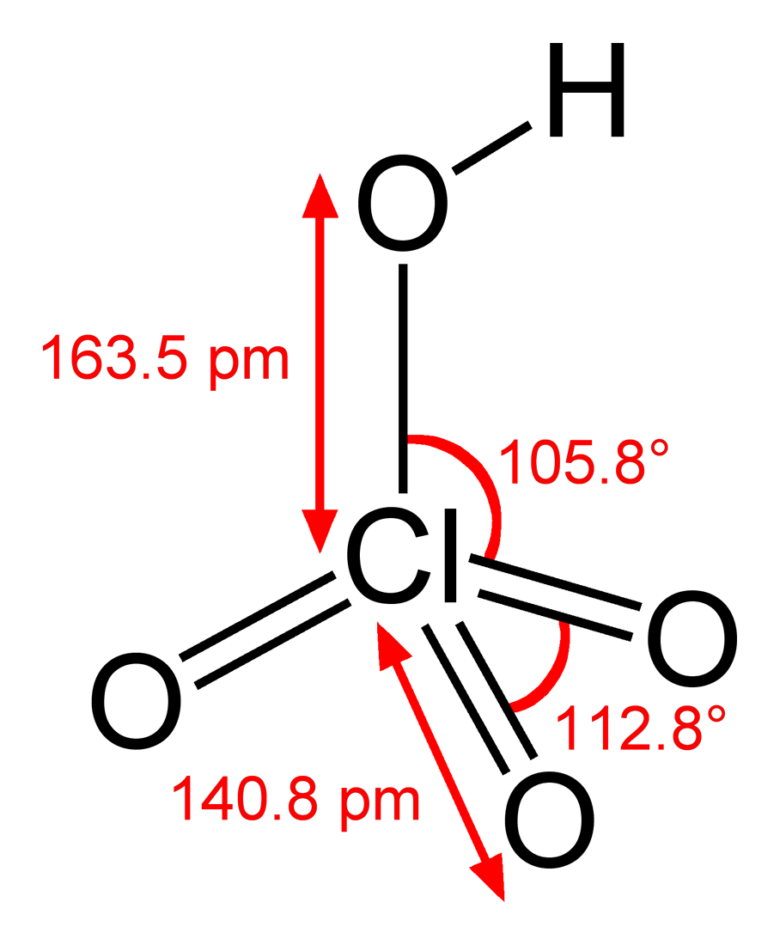
塩素のオキソ酸にはHClO、HClO2、HClO3、HClO4の四種類があります。この中で最も酸性が強いのは HClO4 です。
HClO4 の中心にあるCl原子は周囲のOから電子を取られ、電子が極端に足りない状態になっています(酸化数+7)。つまり、ここには電子が入り込む隙間があり、Oの電子がいくらか流入します。その結果、Hの電子がOにより奪われることになり、H+として非常に電離しやすくなります。

Cl原子から電子が取られ過ぎて、空きができすぎて、逆にOの電子を引き寄せるんだね。

塩素のオキソ酸にはHClO、HClO2、HClO3、HClO4の四種類があります。この中で最も酸性が強いのは HClO4 です。
HClO4 の中心にあるCl原子は周囲のOから電子を取られ、電子が極端に足りない状態になっています(酸化数+7)。つまり、ここには電子が入り込む隙間があり、Oの電子がいくらか流入します。その結果、Hの電子がOにより奪われることになり、H+として非常に電離しやすくなります。

Cl原子から電子が取られ過ぎて、空きができすぎて、逆にOの電子を引き寄せるんだね。