最外殻の電子は2つだけどFe3+になった方がより安定するから
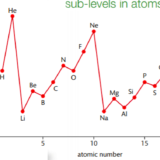
鉄の電子配置を書いてみましょう。K、L、M、N殻をさらに細かく書くと次のようになります。
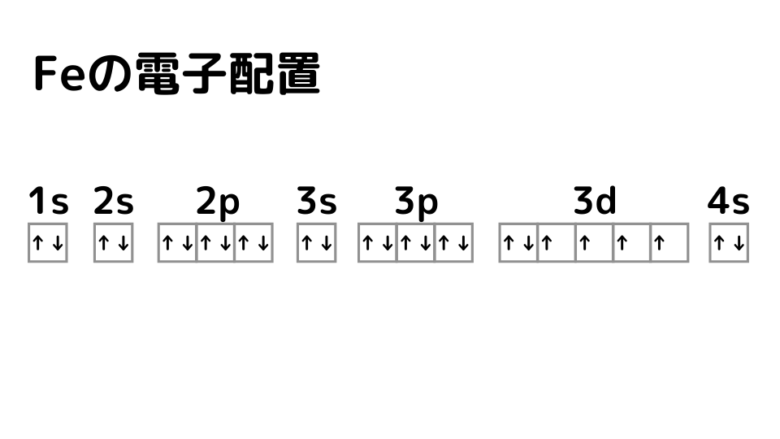
鉄がイオンになる際には、初めに一番外側の電子2個が放出されます。電子が二個放出されると、微妙な状態で電子が埋まっている3d軌道が出現します。これがFe2+の状態です。
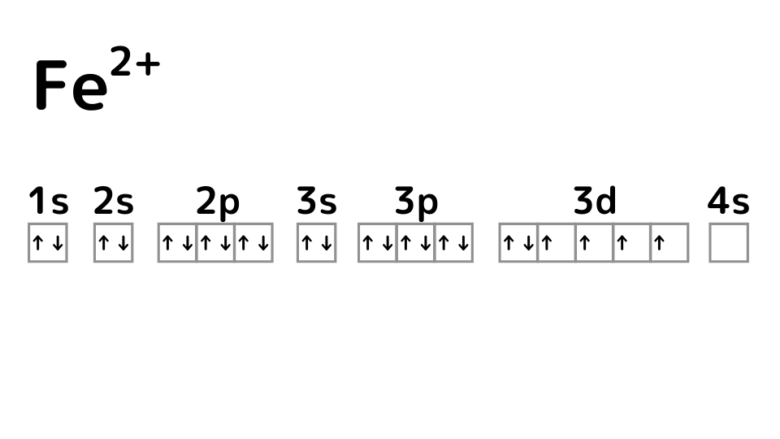
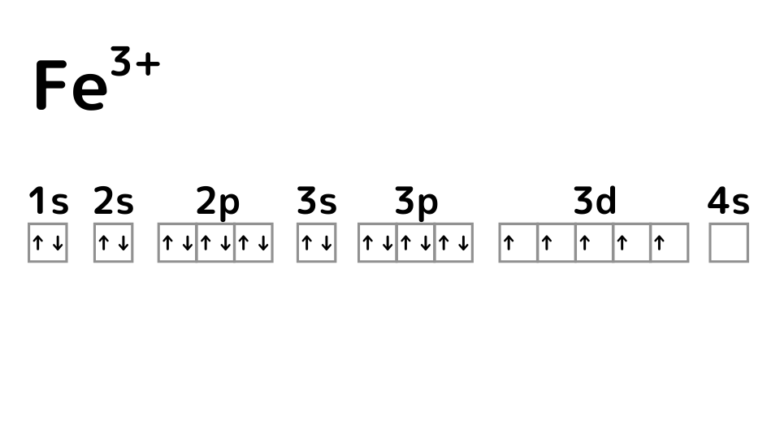
3d軌道が中途半端なので、Fe2+は電子をもう1つ放出しようとします。3d軌道の電子が1つ放出されると、3d軌道は半閉殻状態となり安定します。Fe3+は比較的安定したイオンとして存在します。
こんな感じで、Fe2+は電子を放出する性質(還元作用)が強いため、代表的な還元剤として知られています。

Feが最外殻の電子を放出してFe2+になっても、もう1つ電子を放出した方が安定できるからFe3+にもなるんだね。