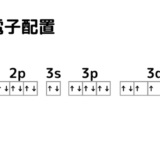
電子軌道から理由が見えてくる
第一イオン化エネルギーとは、中性の原子から電子1個を取り去って陽イオンにするのに必要なエネルギーのことを指します。

基本的に同じ周期ならば、原子番号が大きくなる順に第一イオン化エネルギーも大きくなるのですが、ベリリウムとホウ素は逆転しています。これはなぜしょうか。

電子軌道を見ながら解説するよ
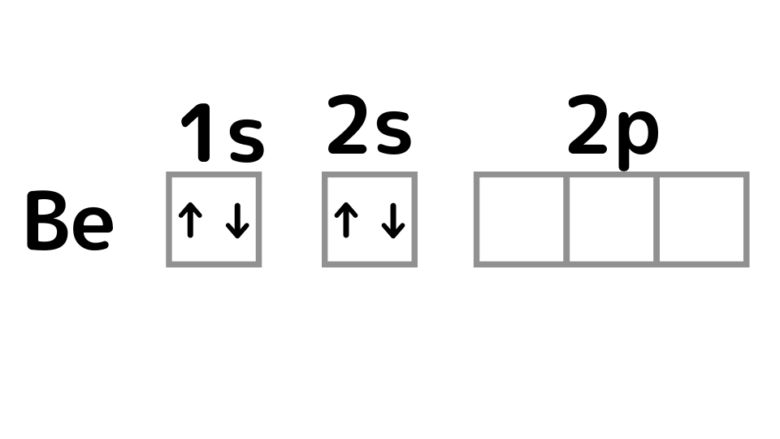
ベリリウムの電子は4つですが、これを電子軌道で書くと次のようになります。↑または↓は電子を示しています。ベリリウムは2s軌道が閉殻しており、この状態から電子を奪うのにはエネルギーを必要とします。
一方、ホウ素の電子軌道は次のようになっています。
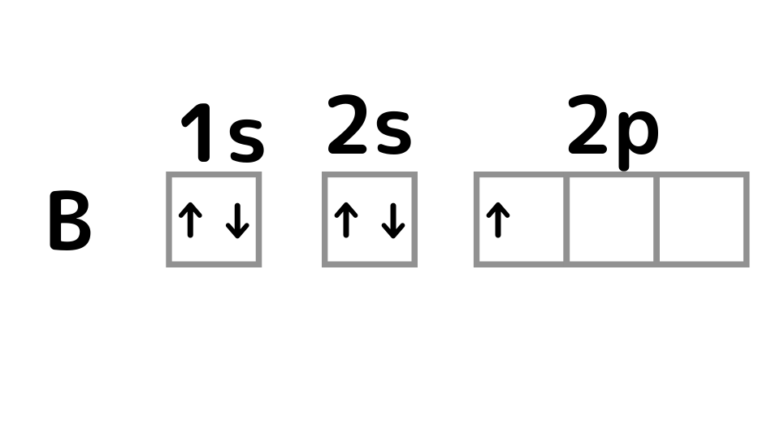
ホウ素は2pに1つだけ電子があるため、この電子を取り除くとBeと同じ2s軌道が閉殻状態になります。つまり、安定した状態となります。
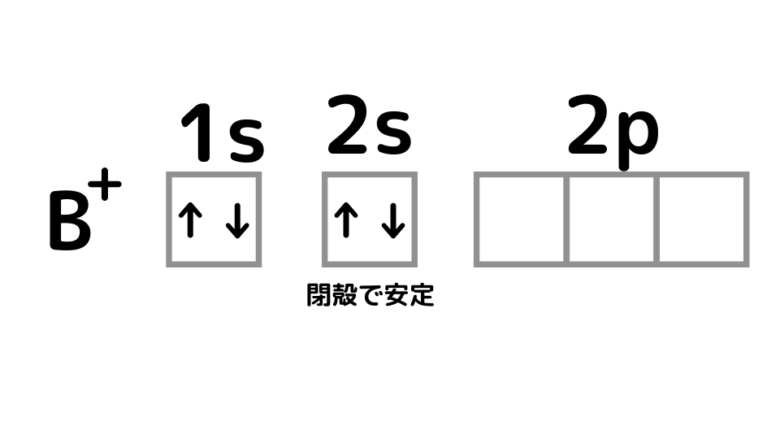
ホウ素の第一イオン化エネルギーが小さかったのは、電子を1個放出すると安定した構造が出てくるため、電子1個がやや放出されやすくなっているというわけです。

自然界ではホウ素は陽イオンにはなりません。あくまで人工的な環境での話だね。
ちなみに、NとOも逆転していますが、理由はこれと全く同じです。