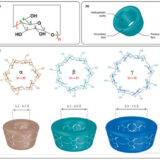
ヨウ素がデンプンのらせん構造の中に入る
デンプンの水溶液にヨウ素液を加えると青~青紫色に呈色します。これをヨウ素デンプン反応と呼びます。
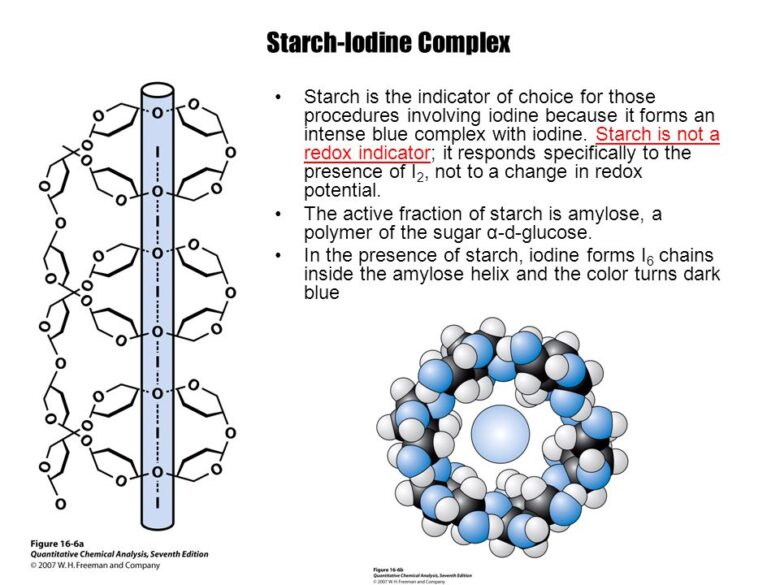
デンプンのらせん構造の中にヨウ素分子が入り込み、ヨウ素が1列に配列して錯体のようなもの(包接化合物)を形成します。すると、電子の豊富な部分から不足した部分への電荷移動がおこり、その結果可視光の吸収が生じて呈色します。
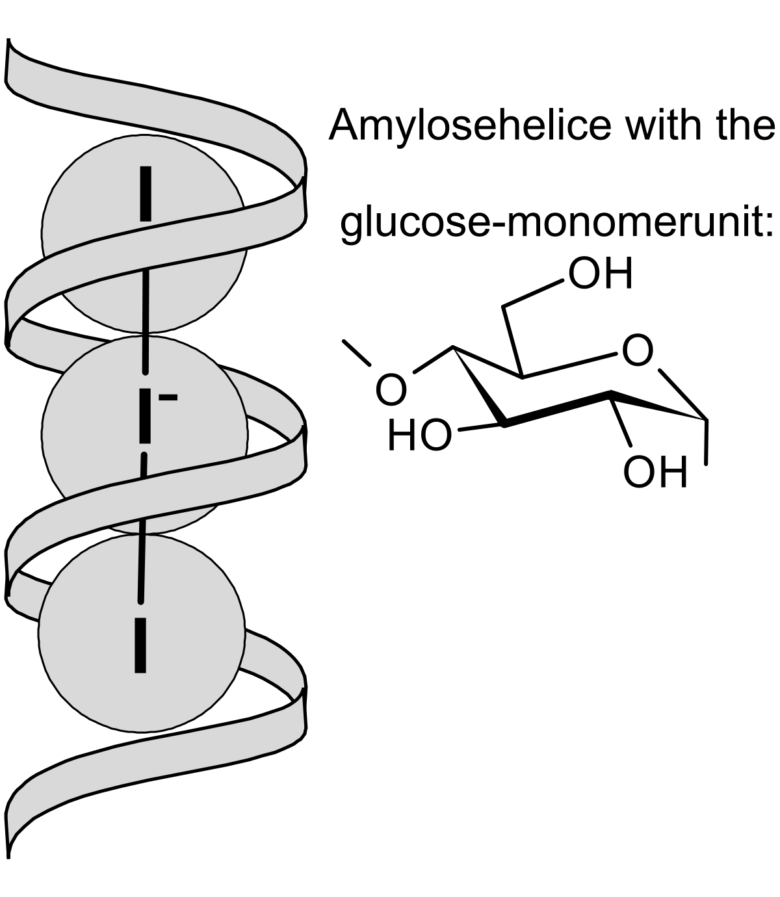
また、らせん構造の中にあるヨウ素の共有結合半径は全て1.53Å で、全てのヨウ素原子が繋がったような特殊な状態にあります。
α-グルコースを模型などでそのまま結合させると、結合角は90度になります。この状態でいるよりも、結合角を110度に広げることでらせん構造を生じさせ、より立体構造的に安定します。そのため、デンプンはらせん構造をとっています。
加熱するとデンプンのらせん構造が崩れ、ヨウ素分子がらせん構造から離れるためです。しかし、冷却するとヨウ素はより安定ならせん構造へと戻るため、再び呈色が見られます。