イオン結晶とは
陽イオンと陰イオンが静電気的なクーロン力によってイオン結合し、粒子が規則立たしくならんだ物質をイオン結晶と呼ぶ。
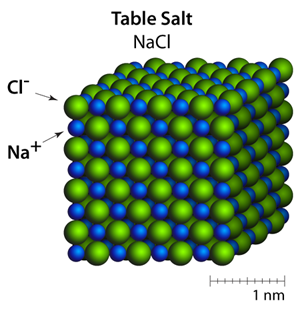
NaClの結晶(イラスト)http://www.atomsinmotion.com/
イオン結晶の性質
イオン結合は+と-の静電気力による結合なので、+- +-+-+-と規則的に並んでいく。その結果、イオン結晶には次の性質がある。
- 硬いが割れやすい
- 融点が高い
- 固体は電気を通さないが、融解した液体は電気を通す
- 水溶液は電気を通す
- 水に溶けやすいものが多い
イオン結晶の結晶格子
イオン結晶の結晶格子は、陽イオンと陰イオンの大きさの違いから、物質によって様々な格子の形を作る。
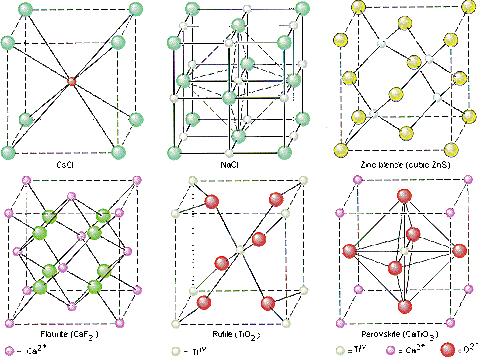
様々な形の単位格子
覚えておくべき単位格子は、NaCl、CsCl、ZnSの単位格子である。構成する原子の個数は、組成式の陽イオンと陰イオンの比と同じである。
NaClの単位格子
Na+ = 4個
Cl- = 4個
配位数 Na+:6、Cl-:6
CsClの単位格子
Cs+ = 1個
Cl- =1個
配位数 Cs+:8、Cl-:8
ZnSの単位格子
Zn2+ = 4個
S2- = 4個
配位数Zn2+ :4、S2-:4
I found your site on tehaonrcti and read a few of your other posts. Keep up the good work. I just added your RSS feed to my Google News Reader. Looking forward to reading more from you.Jason Rakowski